
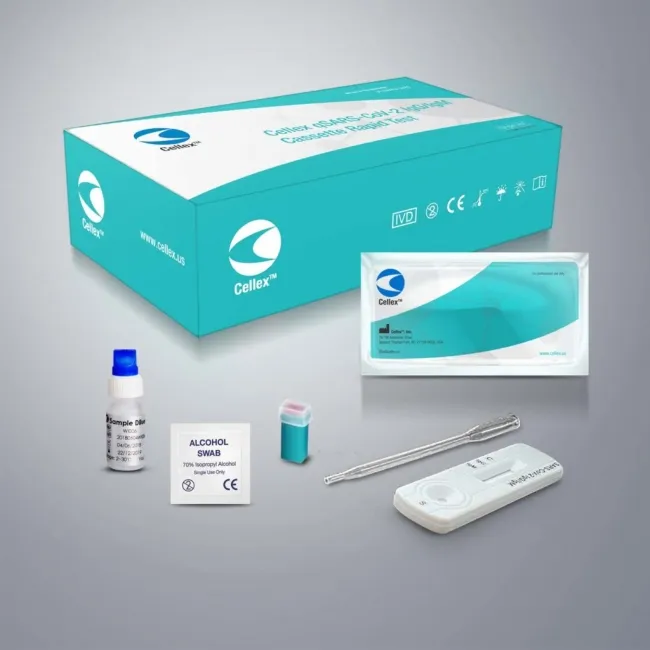
Cellex社の新型コロナウイルス抗体検査キット日本初入荷と販売開始
米国FDAの承認を受けた新型コロナウイルス抗体検査キットの販売開始
米ノースカロライナ州を拠点とするCellex社が開発した新型コロナウイルス抗体検査キット「qSRAS-CoV-2 IgG/IgM Cassette Rapid Test」が、日本において正式に入荷し、販売が開始されます。この製品は2020年4月1日、米国FDAから緊急使用認可(EUA)を取得し、世界に先駆けた抗体検査キットです。
Cellex社の背景と製品の特性
Cellex社は2002年に設立され、医療用検査機器の開発を専門とするバイオテクノロジー企業です。同社の抗体検査キットは、2020年3月25日にはCEマーク(EU加盟国基準適合)も取得しており、米国および欧州においてその臨床的有意性と安全性が認められています。このように高い標準をクリアした製品の日本での導入は、医療機関にとって非常に重要な意味を持つでしょう。
日本における製品の導入状況
当社は医療機関様向けの購買支援サービスを5月14日から開始し、その後、米国からの正規代理認証を5月29日に取得しました。これにより、Cellex社製の抗体検査キットを1,800キット入荷し、25キットを1ケース単位で販売します。価格は購入数に応じて1,650円~2,500円(税別)となります。さらなる2,700キットの入荷も今月内に予定されています。
価格と購入方法
単独購入の場合、900キット以上お買い上げいただくことで、1,650円(税別)でご提供します。共同購入の場合も価格設定があり、購入数に応じて2,500円から1,800円(税別)となります。購入希望者は、当社の公式ウェブサイトを通じて申し込みが可能です。
感染症専門家からの警告
新型コロナウイルス感染症に関しては、5月25日に全国的な緊急事態宣言が解除されました。しかし、多くの専門家は、今後感染拡大の第二波が懸念されると警告しています。このため、抗体検査の需要は日に日に高まっており、信頼性のある製品の入荷は医療機関にとって不可欠です。
最後に
Cellex社の抗体検査キットは、ただの検査ツールにとどまらず、妊娠の可能性や体調の変化をモニタリングする新たな手段ともなり得ます。国内未承認の製品も多く流通する中、信頼の置ける製品の供給が日本の医療現場において企画されていることは、患者様の安全を守る一助となることでしょう。
製品情報
- - 製品名: qSRAS-CoV-2 IgG/IgM Cassette Rapid Test
- - 製造元: Cellex社(米国・ノースカロライナ州)
- - 判定対象: 新型コロナウィルス抗体2種(IgG/IgM)
- - 所要時間: 15分
- - 承認関連: 米国FDA緊急使用認可(EUA)、CEマーク、他
- - 生産地: 中国
- - 保管方法: 室温(2〜30℃)
- - 使用期限: 12ヶ月
さらに詳しい情報や購入に関するお問い合わせは、こちらのリンク からご確認ください。
会社情報
- 会社名
- メディカルエクスポート合同会社
- 住所
- 東京都調布市調布ケ丘2-6-42
- 電話番号
- 080-4637-0240
トピックス(その他)










【記事の利用について】
タイトルと記事文章は、記事のあるページにリンクを張っていただければ、無料で利用できます。
※画像は、利用できませんのでご注意ください。
【リンクついて】
リンクフリーです。