
機能性表示食品の新基準PRISMA2020がもたらす企業の挑戦と展望
機能性表示食品の新基準PRISMA2020がもたらす企業の挑戦と展望
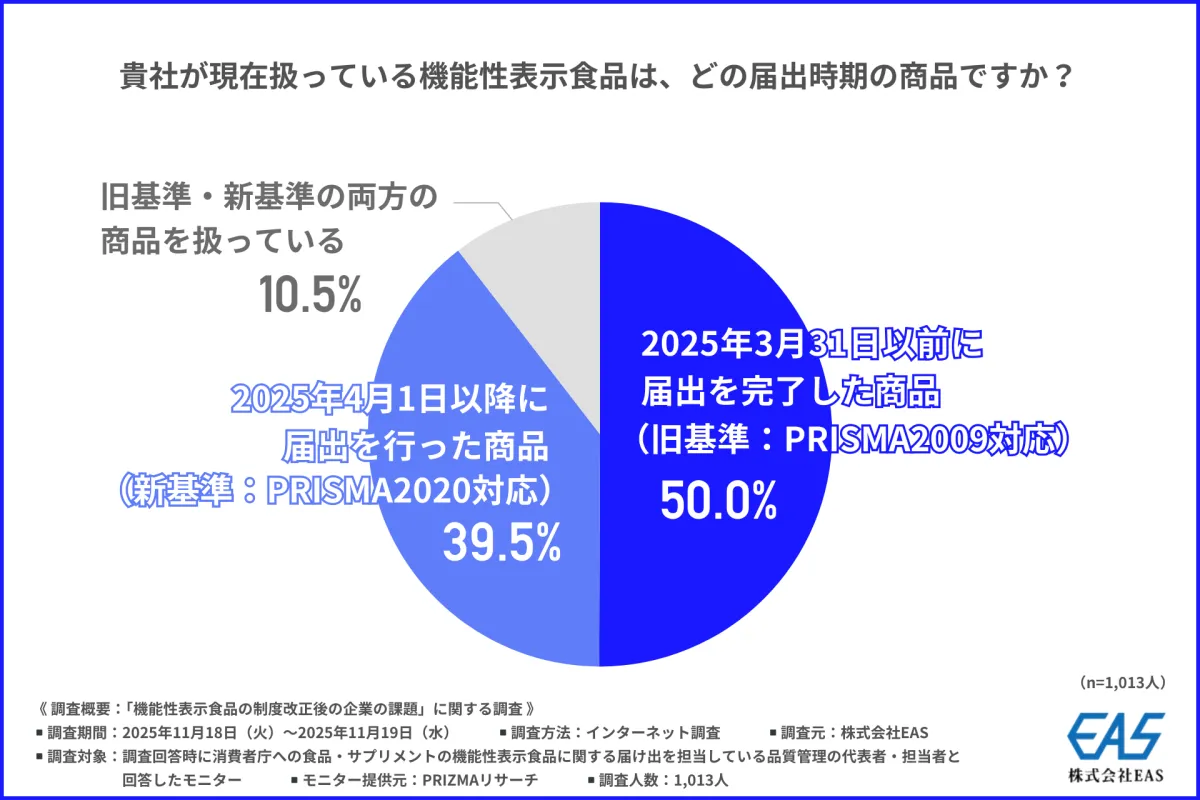
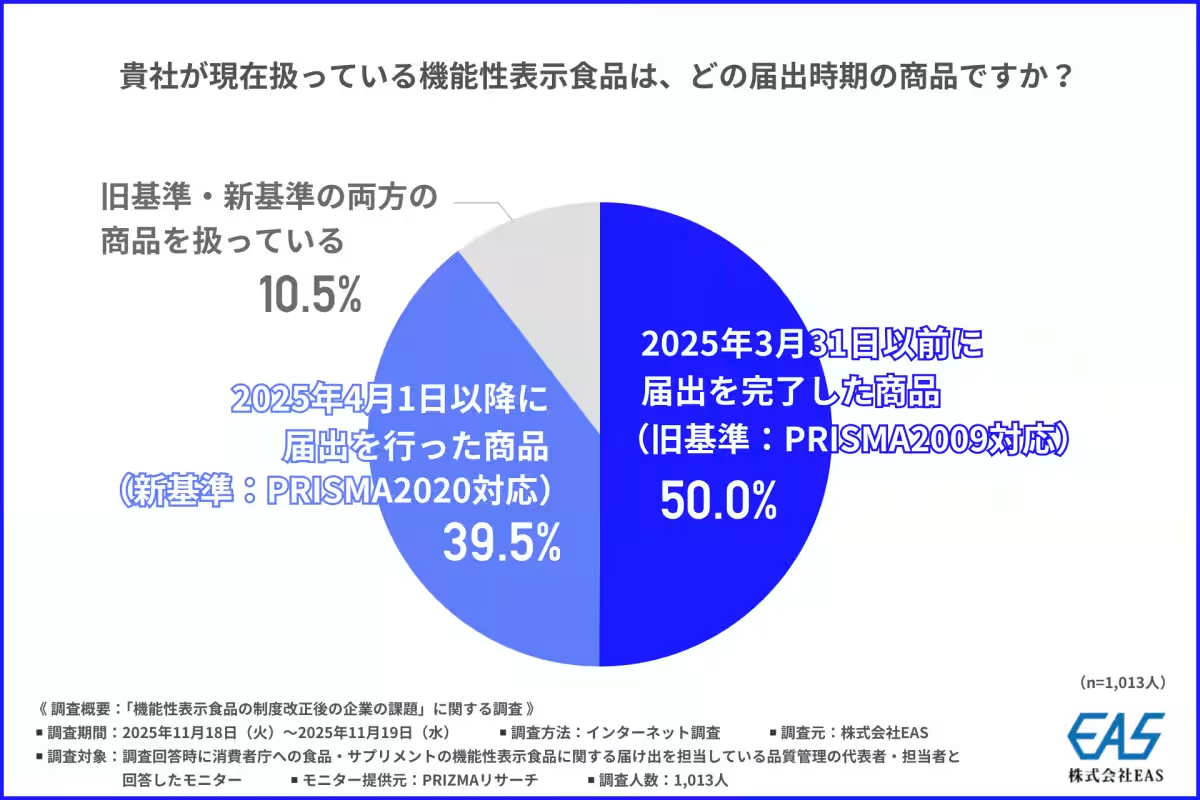
株式会社EAS(本社所在地:神奈川県横浜市)は、食品およびサプリメントの機能性表示食品に関する消費者庁への届け出を行う品質管理担当者を対象に、機能性表示食品制度の改正に対する企業の課題を調査しました。この調査は、近年注目されている紅麹サプリメントの健康被害により、機能性表示食品の「科学的根拠」や「安全性」が改めて問い直される中で実施されました。
PRISMA2020とは何か?
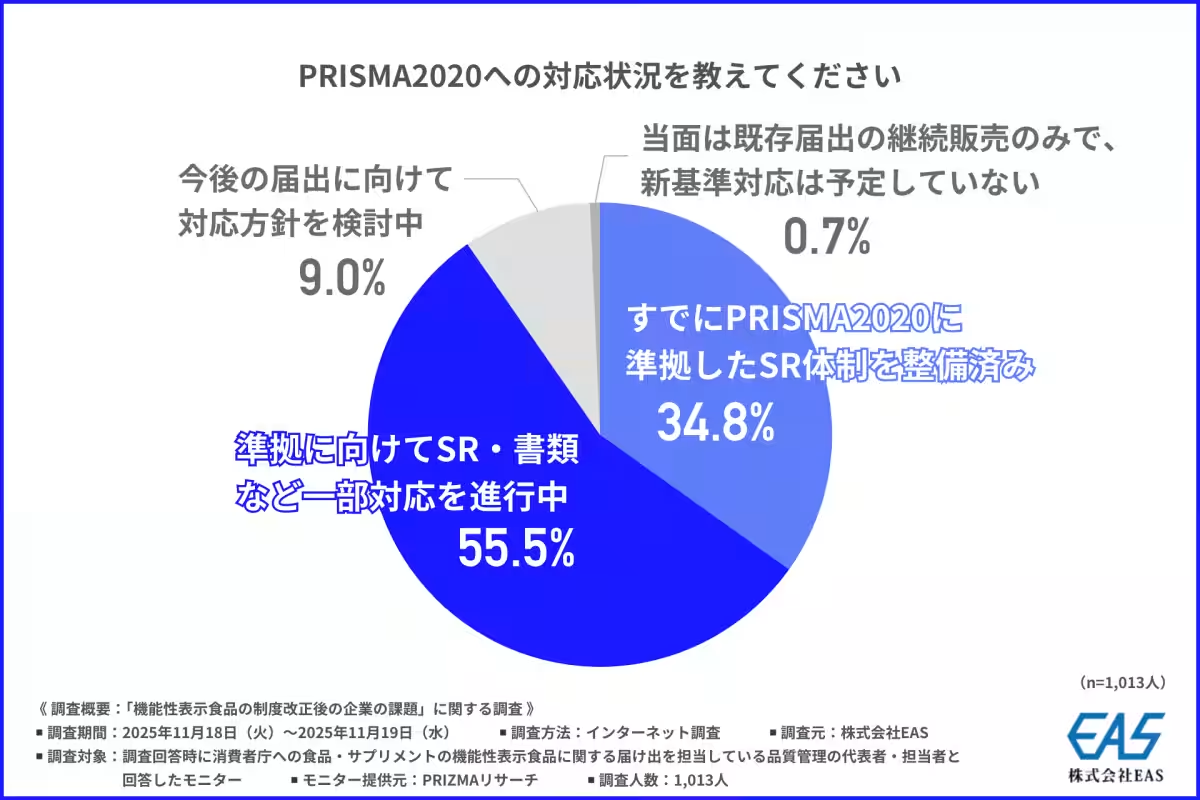
2025年4月に施行予定の新基準PRISMA2020は、エビデンスの透明性向上を目的にシステマティック・レビュー(SR)を求めるものです。この新基準に移行するためには、企業が自らの対応体制を整える必要があります。調査結果によれば、すでにPRISMA2020に準拠したSR体制を整えた企業は34.8%、そして55.5%は現在準備を進めていることが分かりました。
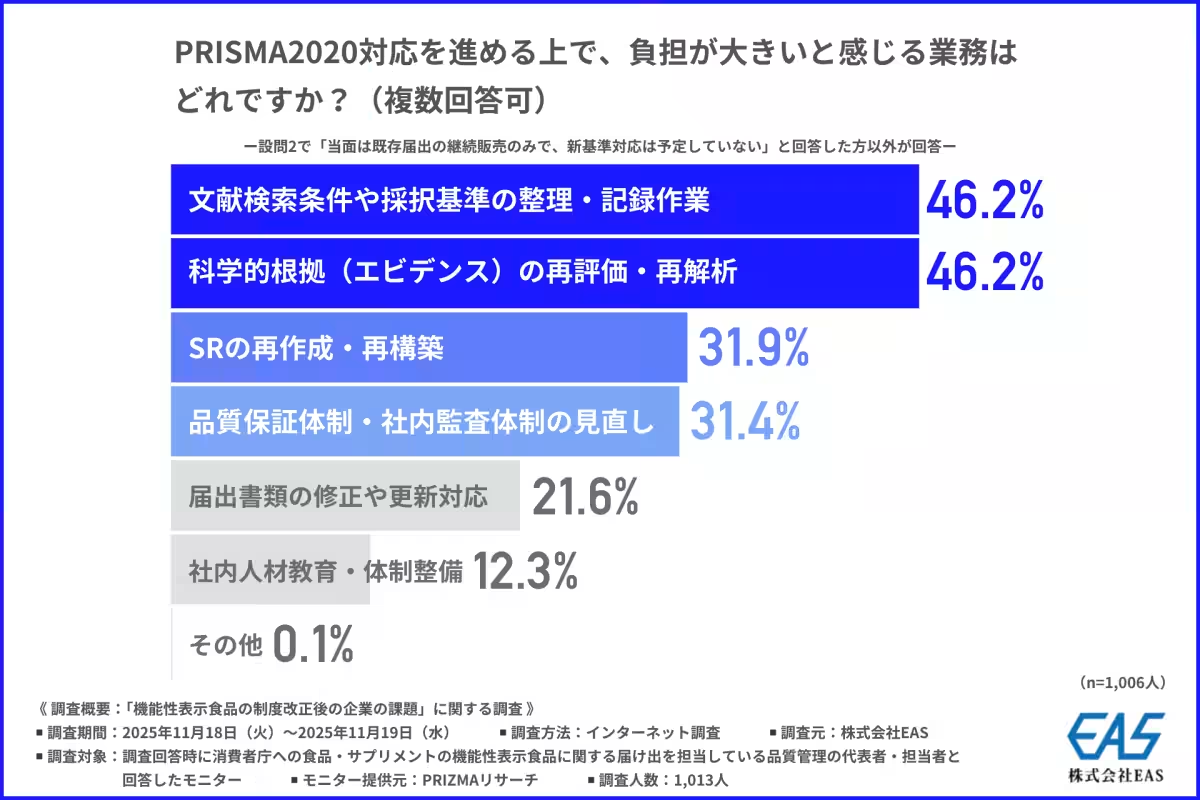
審査・差し戻しへの不安
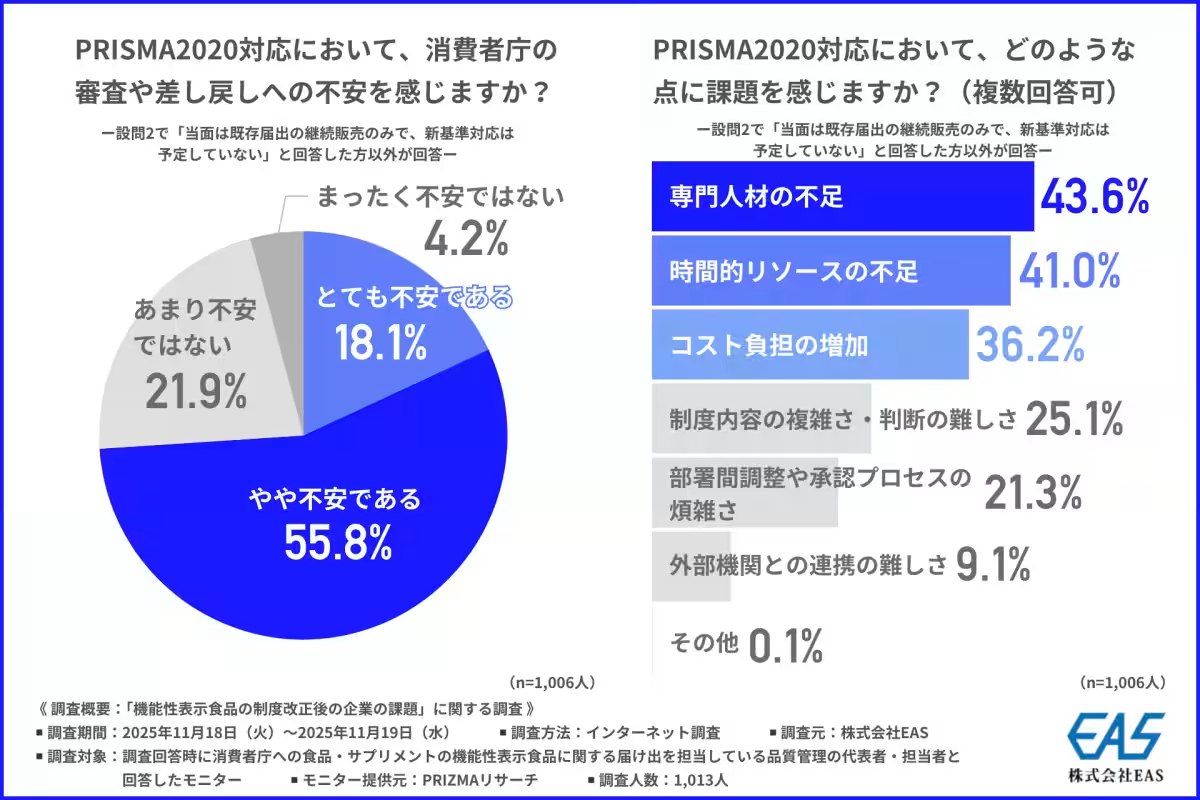
調査によると、約7割の企業が消費者庁の審査に対して不安を感じていると回答しています。これは、設けられた基準の厳格化や解釈の難しさが背景にあると考えられています。具体的には、文献検索の条件整理や科学的根拠の再評価が特に負担を感じる業務として挙げられています。
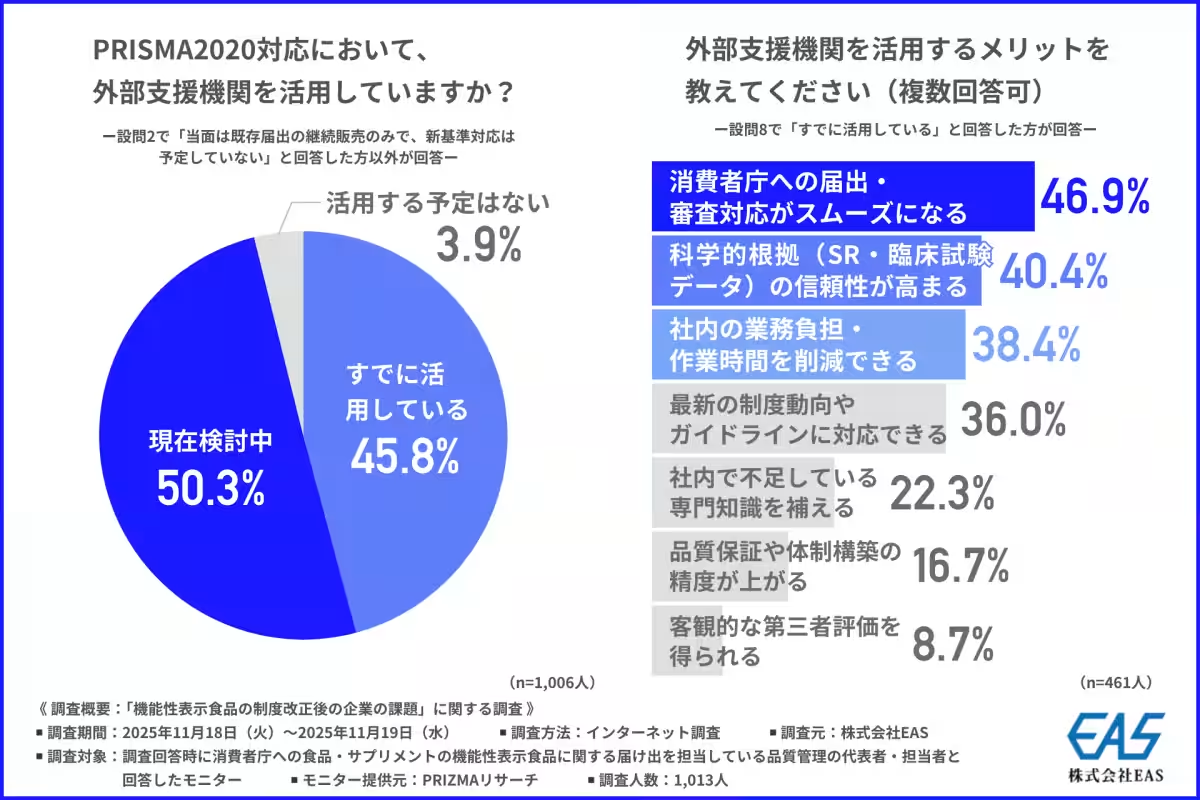
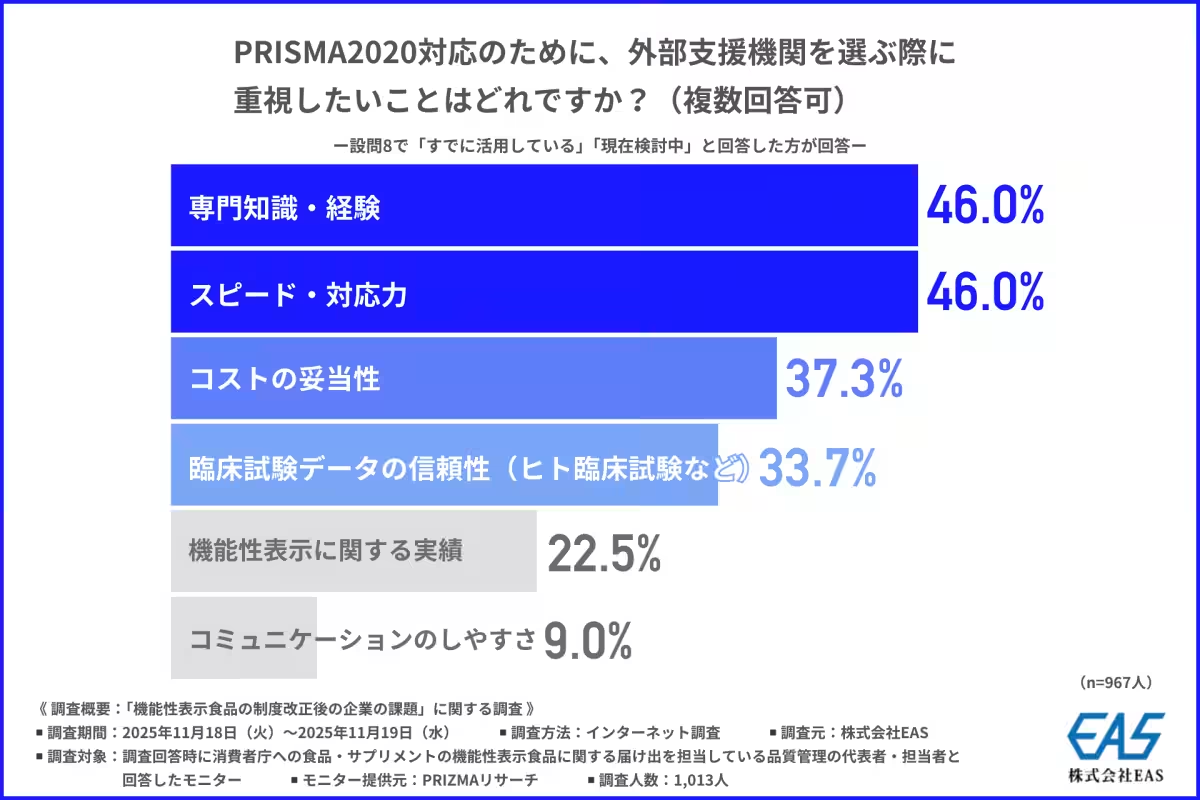
外部支援機関の活用
企業は新基準に対応するために、外部支援機関の活用を進めています。調査結果によれば、91.1%の企業が外部支援機関をすでに活用しているか、検討中であると回答しました。特に、消費者庁への届出や審査対応がスムーズになる点が大きなメリットとされています。企業が直面する専門的な知識や迅速な対応が求められる中で、外部支援機関の重要性が増しています。
企業の未來とPRISMA2020の意義
PRISMA2020への対応は、企業にとってただの義務にとどまらず、信頼性向上や市場競争力の強化にもつながります。企業は専門知識を得るための社内教育やマニュアル整備が求められ、品質保証体制の強化も求められています。こうした対策を講じることで、差し戻しのリスクを低減し、更なる業務の効率化につながるでしょう。
まとめ
機能性表示食品の新基準PRISMA2020に対する移行は企業にとって大きな挑戦です。しかしながら外部支援機関の活用や体制強化を通じて、信頼性や効率の向上が期待できるでしょう。科学的根拠をしっかりと支える力強い外部パートナーの存在は、今後の成功に向けた重要なカギとなるでしょう。
会社情報
本記事で調査を行った株式会社EASは、食品やサプリメントの科学的根拠となるヒト臨床試験データの取得を支援している受託機関です。企業が確かなエビデンスを基にした製品価値を創出できるよう、全面的にサポートしています。

会社情報
- 会社名
- 株式会社EAS
- 住所
- 神奈川県横浜市中区桜木町1-1-7ヒューリックみなとみらい10階
- 電話番号
トピックス(ライフスタイル)










【記事の利用について】
タイトルと記事文章は、記事のあるページにリンクを張っていただければ、無料で利用できます。
※画像は、利用できませんのでご注意ください。
【リンクついて】
リンクフリーです。