
糖鎖合成酵素B4GALNT3の新たな調節メカニズムの発見
糖鎖合成酵素B4GALNT3の新たな調節メカニズムの発見
岐阜大学糖鎖生命コア研究所の木塚康彦教授とその研究グループは、他の大学や研究機関との共同研究を通じて、糖鎖合成酵素B4GALNT3に新しい機能を発見しました。特に、この酵素にはレクチンドメインが存在し、これがタンパク質に付く糖鎖の合成において重要な役割を果たすことが示されました。
研究の背景と目的
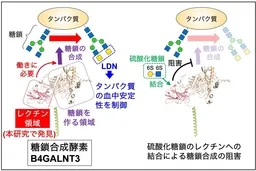
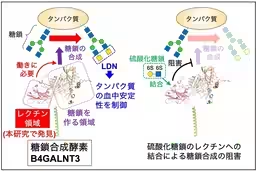
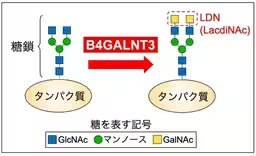
B4GALNT3 は、血中のホルモンやタンパク質の安定性を調節する重要な酵素で、LDNと呼ばれる糖鎖の末端を形成します。これまではB4GALNT3の主要な機能については知られていましたが、その活性をどのように調節するかについてはあまり理解されていませんでした。今回の研究は、B4GALNT3がレクチンドメインを持ち、特定の糖鎖と結合することを明らかにしたことで、この問題に新たな光を当てました。
発見の詳細
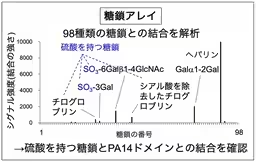
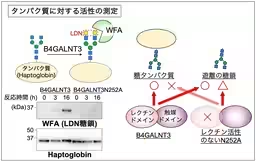
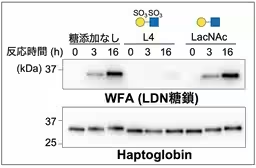
研究チームは、B4GALNT3がレクチンドメインを持っていることを確認しました。このレクチンドメインは、特に硫酸化された糖鎖と結合し、B4GALNT3の糖鎖合成活性を調節することが判明しました。具体的には、レクチンが糖鎖と結合することでB4GALNT3の活性が抑制されるという仕組みが確認されました。これにより、B4GALNT3の糖鎖合成の機能が、周囲の糖鎖の種類や構造に依存して調節されることが分かりました。
研究方法
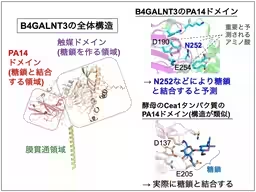
本研究では、B4GALNT3のPA14ドメインが物質と結合するかどうかを調べました。このドメインがレクチンとして機能するかを確認するために、様々な糖鎖を用いた結合実験が行われました。その結果、硫酸化糖鎖との結合が確認され、特に重要なアミノ酸が明らかになりました。
重要性と今後の展望
B4GALNT3のレクチンドメインの発見は、糖鎖がどのように合成され、なぜ特定の条件下で変化するのかを理解する上で重要な知見となります。この成果は、ホルモン調節や骨形成といった生理的プロセスへの理解を深めるものであり、今後の研究により、糖鎖の調節機構が解明されることが期待されます。さらに、これらの結果は医療における糖鎖の臨床応用にも繋がる可能性があります。
結論
本研究は、B4GALNT3が持つレクチンドメインの役割を明らかにしただけでなく、この発見が細胞内での糖鎖合成調節や病態における糖鎖の変化に関するさらなる研究へと繋がる礎を築くものです。今後、糖鎖に関する新たな知見が、医療の進展に貢献することを願います。
会社情報
- 会社名
- 岐阜大学
- 住所
- 電話番号
トピックス(科学)









【記事の利用について】
タイトルと記事文章は、記事のあるページにリンクを張っていただければ、無料で利用できます。
※画像は、利用できませんのでご注意ください。
【リンクついて】
リンクフリーです。