
国産HAT細胞活用による高品質AAV製造技術の確立
国産HAT細胞による高品質AAV製造技術の確立
はじめに
遺伝子治療は現代医療において革新的な分野として急速に発展し、その治療の鍵を握るのがウイルスベクター、特にアデノ随伴ウイルス(AAV)です。これまでAAVの製造には、主にヒト由来のHEK293細胞や昆虫細胞が用いられてきましたが、双方にはそれぞれ特有の課題が存在します。それを打破する新たな技術として、国産のヒト由来細胞株「HAT細胞」が期待されています。
研究成果の概要
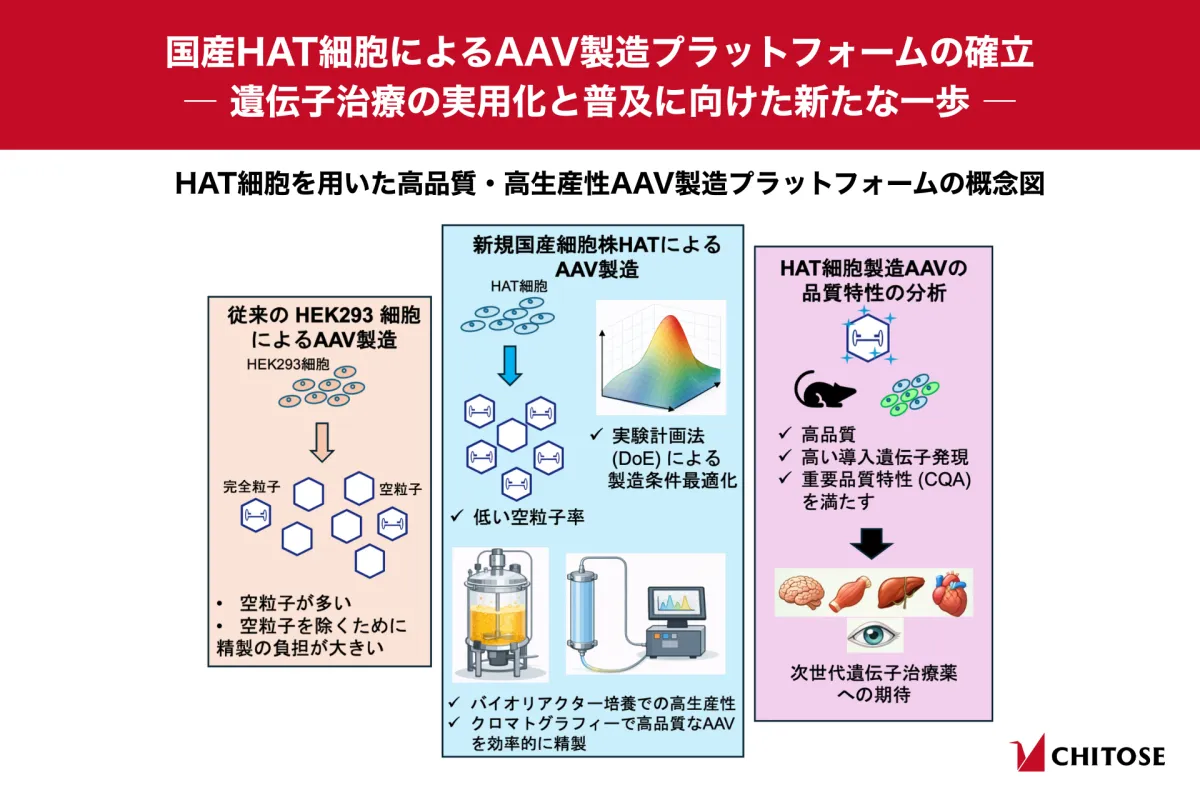
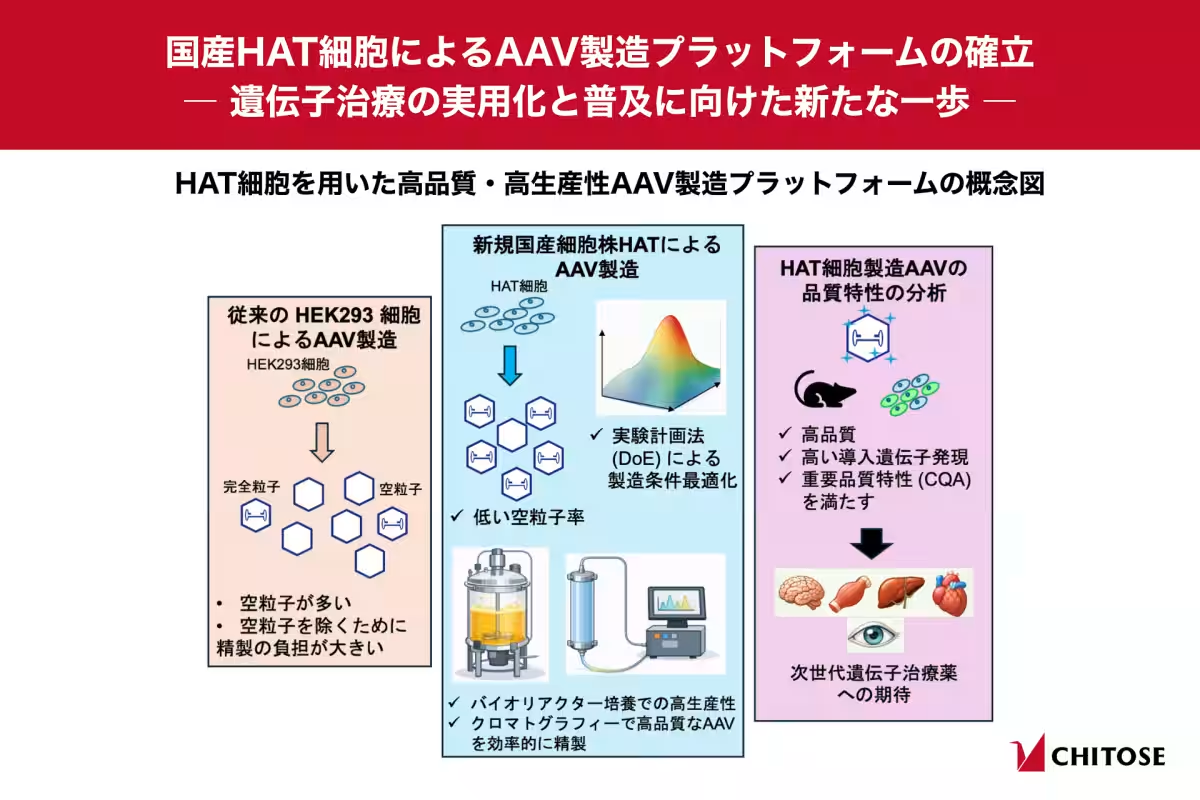
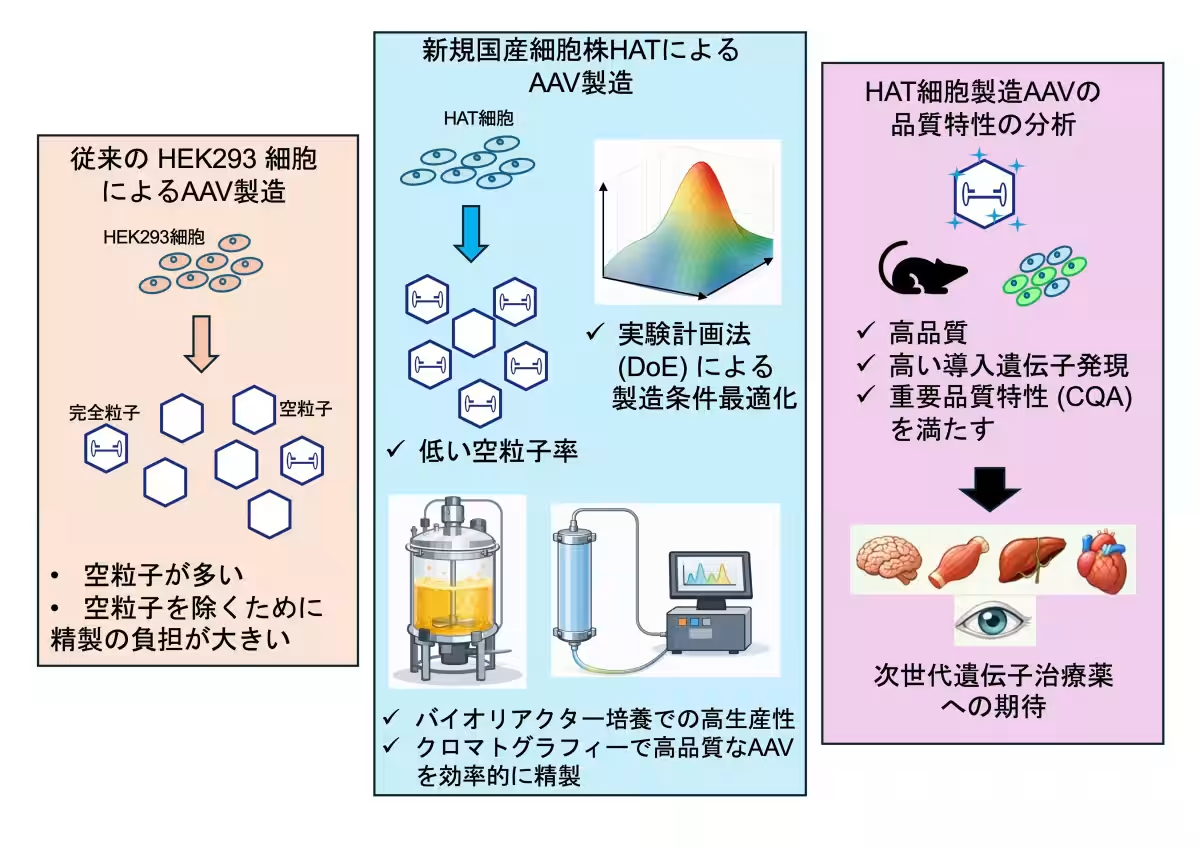
大阪大学の研究チームは、HAT細胞を用いることで、高生産性を維持しながらも、空粒子の生成を大幅に抑えたAAV製造プラットフォームを世界で初めて確立しました。この成果は、株式会社ちとせ研究所や自治医科大学などとの共同研究によってもたらされたものです。
従来の課題
遺伝子治療用のAAV製造においては、生産性と品質を両立させることが難しく、特に治療効果を持たない空粒子の生成が大きな障壁となっていました。空粒子は、患者に投与される薬剤の有効性を低下させる可能性があるため、製造過程での除去が不可欠です。
HAT細胞の利点
HAT細胞は、ヒトの胎盤に由来する羊膜上皮細胞を基に開発された細胞株で、優れた増殖性能とウイルスベクターの安定的な供給能力を持っています。この研究では実験計画法(Design of Experiments:DoE)を用いて生産条件の最適化を図り、空粒子生成を抑えつつ、AAVの高い生産性を維持しました。
研究の詳細
研究チームは、HAT細胞をバイオリアクターで培養し、AAVを製造しました。その結果、従来のHEK293細胞由来のAAVと比較しても遜色ない、あるいはそれを上回る高い品質特性を持つAAVを得ることに成功しました。具体的には、空粒子率や翻訳後修飾に関する評価を行い、HAT細胞由来のAAVが優れた特性を示すことを確認しました。
社会に対する意義
この研究成果により、遺伝子治療薬の製造コストを低減し、安定した供給が可能になることで、希少疾患を含む多様な遺伝子治療薬の臨床開発が進むことが期待されています。また、HAT細胞を用いたアプローチは、科学療法の分野への応用も見込まれています。
今後の展望
今後、産学官連携を通じてこの技術の実用化を進め、日本の遺伝子治療薬製造エコシステムの確立を目指します。最適な製造条件の明確化や重要品質特性の評価が、商用製造への円滑な移行を可能にし、国際競争力の強化に寄与することでしょう。
まとめ
本研究は遺伝子治療薬の実用化に向けた新たな方向性を示すものであり、国産化による安定供給体制の構築が期待されます。これにより、より多くの患者へ高品質な治療が提供されることを願っています。




会社情報
- 会社名
- Chitose Bio Evolution Pte. Ltd.
- 住所
- 神奈川県川崎市高津区坂戸3-2-1KSP R&D棟C432
- 電話番号
- 044-813-3380
トピックス(科学)








【記事の利用について】
タイトルと記事文章は、記事のあるページにリンクを張っていただければ、無料で利用できます。
※画像は、利用できませんのでご注意ください。
【リンクついて】
リンクフリーです。