

骨髄移植後を支える新技術、静岡県の支援で実用化へ
静岡県内での新たな医療技術の実用化
2025年12月23日、株式会社TL Genomicsが骨髄移植後の治療経過を評価する革新的な技術が静岡県の「ファンドサポート事業」に採択されたことが報じられました。この技術は、骨髄移植後の再発兆候を高精度で把握できる「キメリズム検査」に焦点を当て、高感度・低コストを両立させることを目指しています。今後は静岡県内で体外診断用医薬品の製造拠点を新設し、2026年4月を目指して実用化に向けた活動を本格化させます。
骨髄移植における検査体制の課題
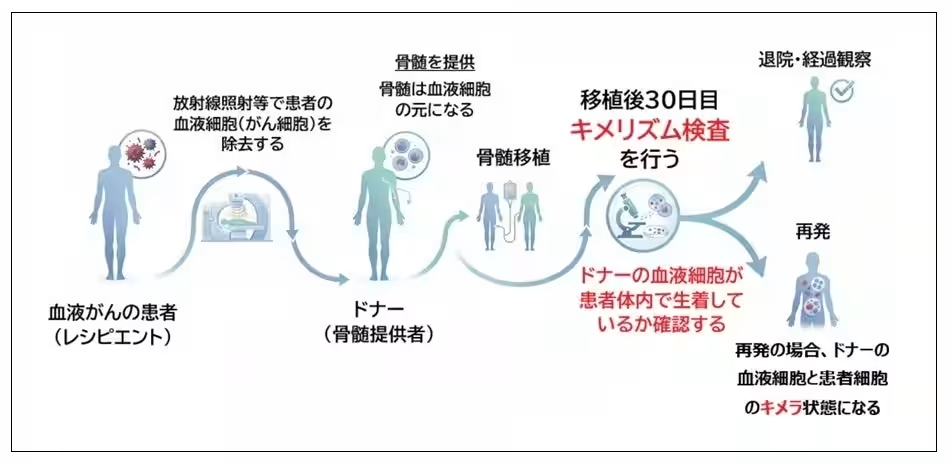
骨髄移植は血液がん治療の重要な手段ですが、移植後には再発の兆候を的確に把握するための検査が求められています。しかし、日本国内には、保険適用検査が存在しないため、多くの患者が再発への不安を抱えながら長期的な経過観察を続けているのが現状です。この問題を解決するために、TL Genomicsの新技術が開発されました。
競合技術との違い
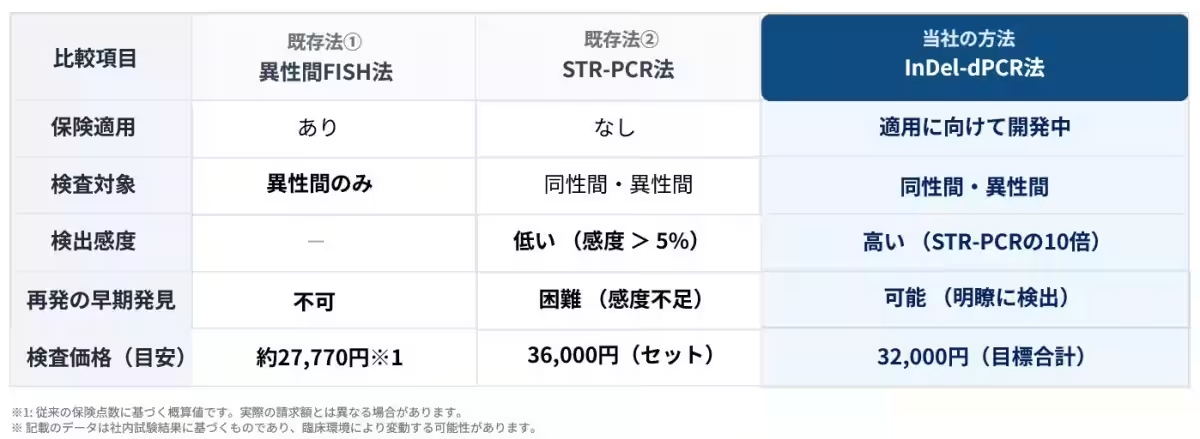
従来の検査方法には、特定条件下でのみ使用可能だったり、感度が低く早期発見が難しいといった課題がありました。しかし、TL Genomicsが開発した「InDel-dPCR法」は、同性間移植に対応しつつ検出感度を大幅に向上させることに成功しました。この新しい検査法によって、再発の見逃しを防ぎ、患者の心理的な負担を軽減する可能性が広がります。
自宅で手軽に検査できるPOCT
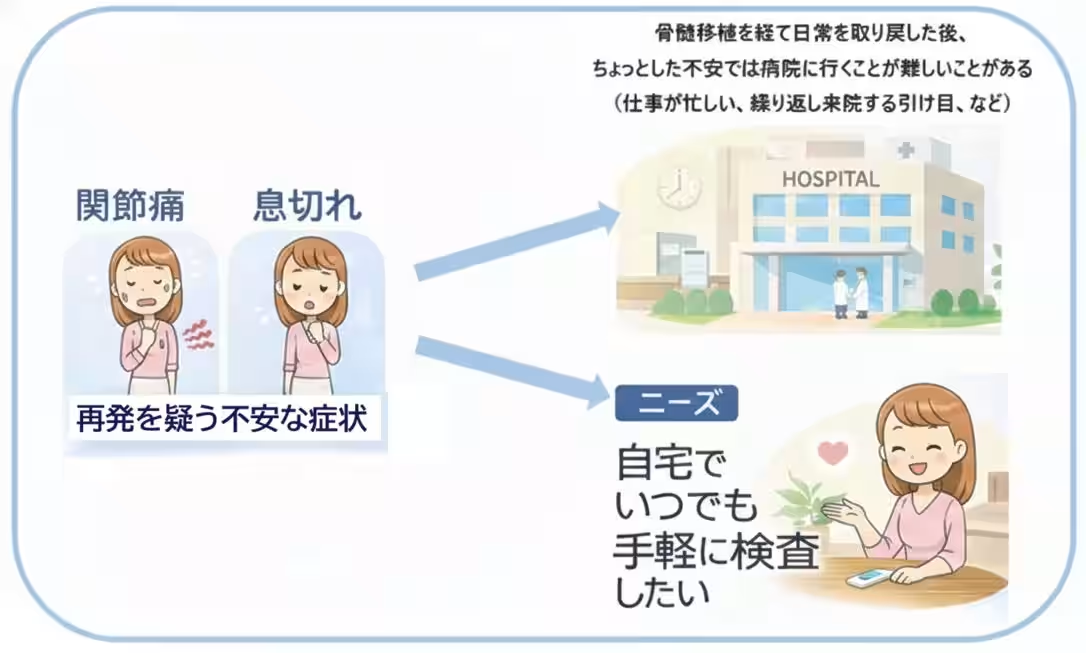
新技術によって、自宅でも簡単に状態を確認できるPOCT(Point of Care Testing)検査が実現します。骨髄移植後の患者は日常生活に戻る際に、時折息切れや関節痛を感じることがあり、再発を心配する場面も多いです。しかし、通院や検査への心理的・時間的な負担から、すぐに病院に行くことが難しい場合もあります。この点で、POCT検査は日常の中で自身の健康状態を把握する手助けとなります。
大阪大学との共同研究を経ての成果
TL Genomicsは、大阪大学との共同研究を進め、従来の検査法に比べておよそ10倍の検出感度を実現し、コストも海外製品の約1/20に抑えたという成果をあげています。この事業は、日本造血・免疫細胞療法学会より支援研究に認定され、臨床研究でも100症例が行われ、その臨床的有用性が確認されています。
目指す未来
今回の採択は、安定した資金を基に自社の技術を実用化し、国内初の保険適用を目指しています。体外診断用医薬品は大規模な工場を必要とせず、地域の医療技術を支えるモデルケースとなることも期待されています。TL Genomicsは、静岡県から始まるこのプロジェクトを通じて、患者の不安を軽減し、より良い医療の質向上に寄与することを目標としています。
会社概要
- - 会社名: 株式会社TL Genomics
- - 所在地: 神奈川県藤沢市遠藤2020-5
- - 設立: 2015年1月
- - 事業内容: 骨髄移植に関する検査・診断薬開発など
連絡先は広報担当の瀬川さんまで([email protected])。


会社情報
- 会社名
- 株式会社TL Genomics
- 住所
- 神奈川県藤沢市遠藤2020-5湘南藤沢インキュベーションLABO #3
- 電話番号
- 0466-47-8655
トピックス(地域情報)










【記事の利用について】
タイトルと記事文章は、記事のあるページにリンクを張っていただければ、無料で利用できます。
※画像は、利用できませんのでご注意ください。
【リンクついて】
リンクフリーです。