
医療機器のグローバル展開を支える最新レポートの概要
医療機器のグローバル展開を支える最新レポートの概要
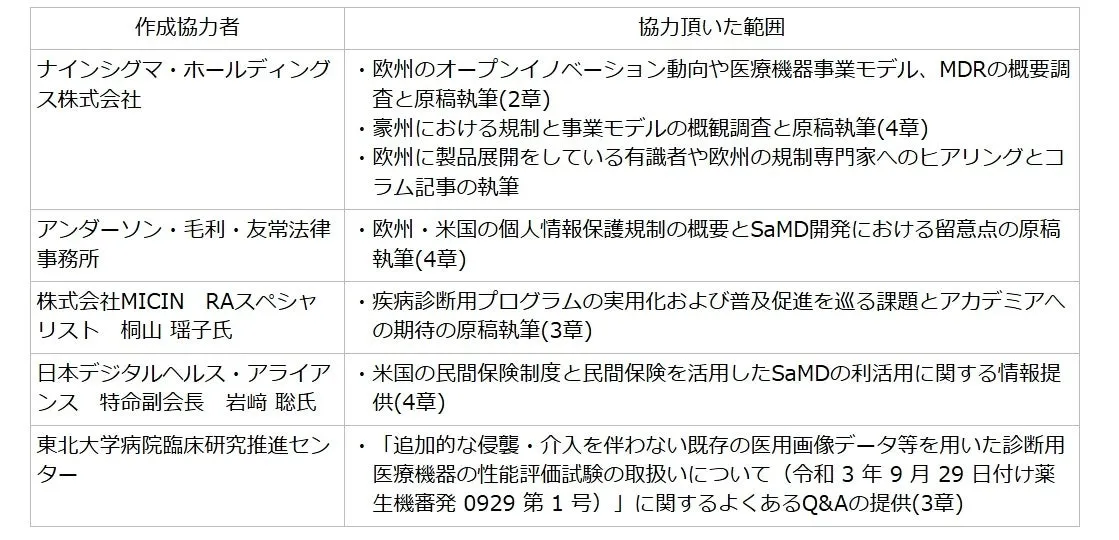
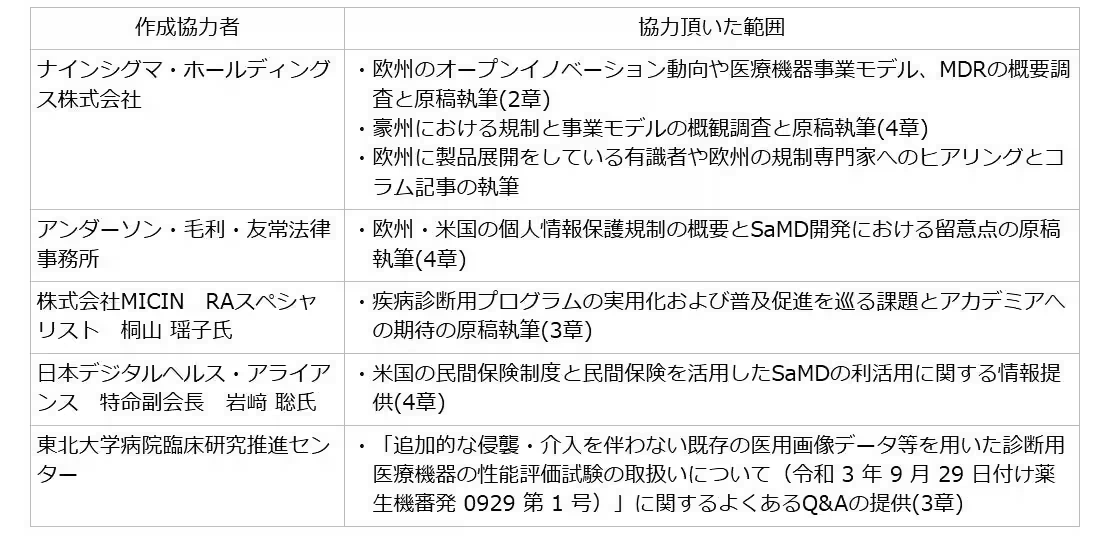
株式会社日本総合研究所は、医療機器産業のグローバルな展開をテーマにした詳細なレポート「医療機器のグローバル展開・プログラム医療機器開発に向けての視座」を発表しました。特にプログラム医療機器(SaMD)に焦点を当て、各国の規制や制度を調査・整理した内容が含まれています。このレポートは、日本医療研究開発機構からの委託を受けて作成され、医療機器の開発や海外展開を円滑に進めるための貴重な情報源となっています。
公表の背景
2024年3月に発表された「医療機器産業ビジョン2024」では、医療機器の海外進出と資金の確保に関する基礎方針が示されました。特に、新技術の開発が進むプログラム医療機器への注力が求められています。この中で、日本企業が海外市場に参入する際の事業機会を見極め、薬事規制や保険制度の特徴を理解することが重要になることが強調されています。
レポートの主要な構成
本レポートは、以下の3部構成でなっています:
1. 欧州の規制に基づく医療機器開発の視点
2. 国内におけるSaMD製品のビジネス実態と薬事戦略
3. 海外のSaMD製品に関するビジネスの実態と戦略
欧州市場の機会
レポートでは、特に欧州における医療機器ベンチャーの資金調達の動向を詳しく分析しています。資金が集う疾患領域や製品領域に関する洞察を提供し、欧州市場におけるプロダクト開発に関する重要な示唆を提示しています。また、オープンイノベーションを積極的に展開する企業の戦略についても詳述しています。
医療機器規制の理解
欧州医療機器規則(MDR)の全貌と、日本と異なるポイントを整理しています。医療機器の分類、安全性や性能要件、臨床評価についても詳細に解説し、早期段階からの規制の理解が重要であると強調しています。
国内のSaMDの実態
日本におけるプログラム医療機器の保険償還制度に関する最新の状況も詳解しています。診療報酬における評価基準や、具体的な保険償還の事例についても取り上げ、政策の変化に伴う特記事項を明らかにしています。
個人情報保護規制への配慮
医療機器開発には個人情報保護の遵守が不可欠です。日本と欧州、米国の規制の違いを示し、具体的な適用分野や事例を紹介しています。自社製品の開発に関しては、各国の規制を意識した慎重な設計が求められます。
米国の民間保険制度
米国における民間保険制度の仕組みを解説し、診療報酬と保険制度の複雑さについても触れています。保険者が給付対象とするSaMDの詳細や、保険適用を受けるためのプロセスについても説明しています。
まとめ
このレポートは、日本企業が医療機器のグローバル展開を成功させるための具体的な視点と情報を提供しており、将来的なビジネスチャンスを見据えた戦略策定に役立ちます。医療機器のグローバル化を目指す企業や研究者にとって、貴重なリソースとなることでしょう。
レポートは以下のリンクから見ることができます。
医療機器のグローバル展開・プログラム医療機器開発に向けての視座
会社情報
- 会社名
- 株式会社日本総合研究所
- 住所
- 東京都品川区東五反田2-18-1大崎フォレストビルディング
- 電話番号
- 03-6833-0900
トピックス(地域情報)










【記事の利用について】
タイトルと記事文章は、記事のあるページにリンクを張っていただければ、無料で利用できます。
※画像は、利用できませんのでご注意ください。
【リンクついて】
リンクフリーです。