
生成AI「CellScribe」が新薬開発を加速!細胞地図の進化と未来
生成AI「CellScribe」が新薬開発を加速!
最近、株式会社ヒューマノーム研究所が開発したシングルセル遺伝子発現量基盤モデル「CellScribe」が注目されています。このモデルは、医薬品の効果や副作用を高精度で予測することを可能にし、創薬研究に大きな影響を与えるでしょう。
新薬開発の課題
新薬の研究開発には、通常10年以上の時間と1000億円以上の投資が必要です。特に、mRNA医薬品や抗体医薬などの新規モダリティは、過去の実験データが少なく、薬剤候補の影響を予測するのが難しいという特徴があります。ここで、細胞単位での遺伝子の活動を詳細に解析するシングルセル技術が、活用されるべきとされています。
シングルセル解析の進化
シングルセル解析は、細胞ひとつひとつの遺伝子発現を捉える技術であり、その進化には目を見張るものがあります。しかし、シングルセルからのデータは非常に膨大で複雑です。これを最大限活用するためには、高効率かつ高精度な解析基盤が必要です。
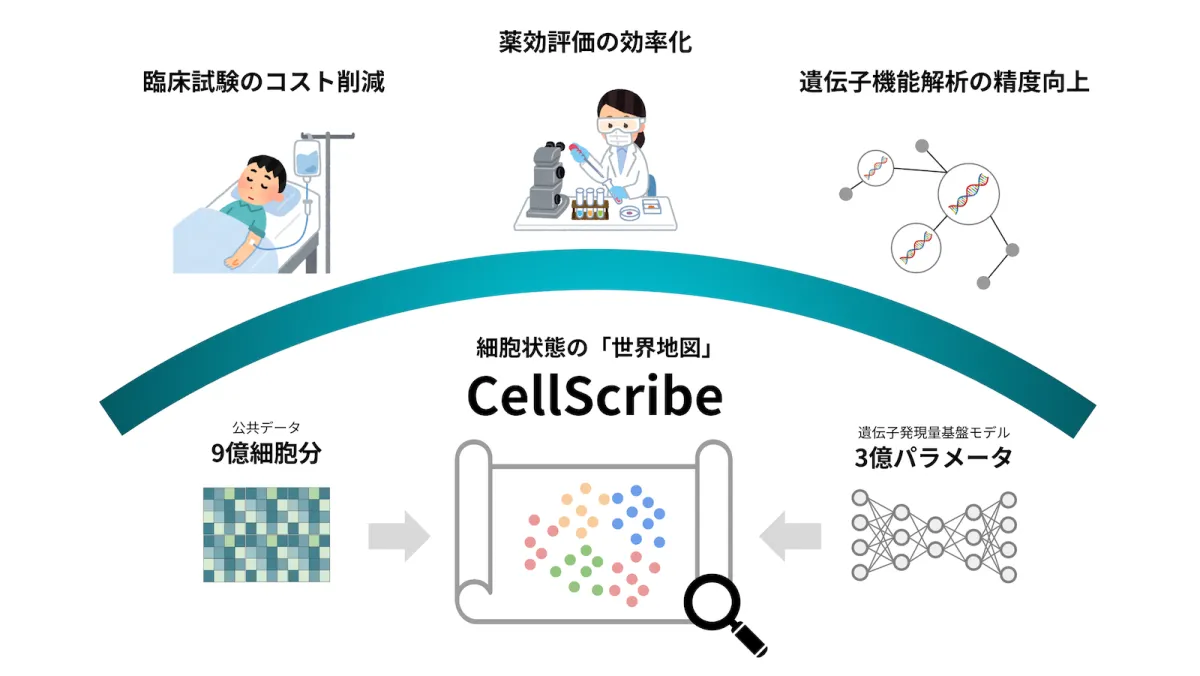
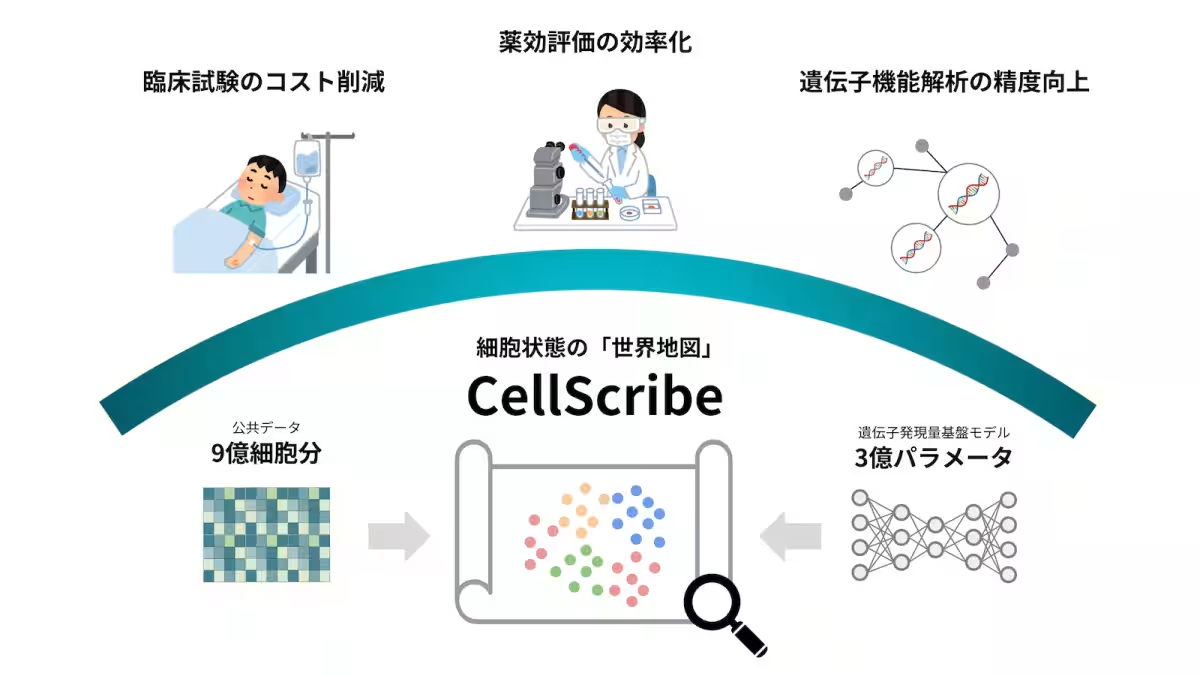
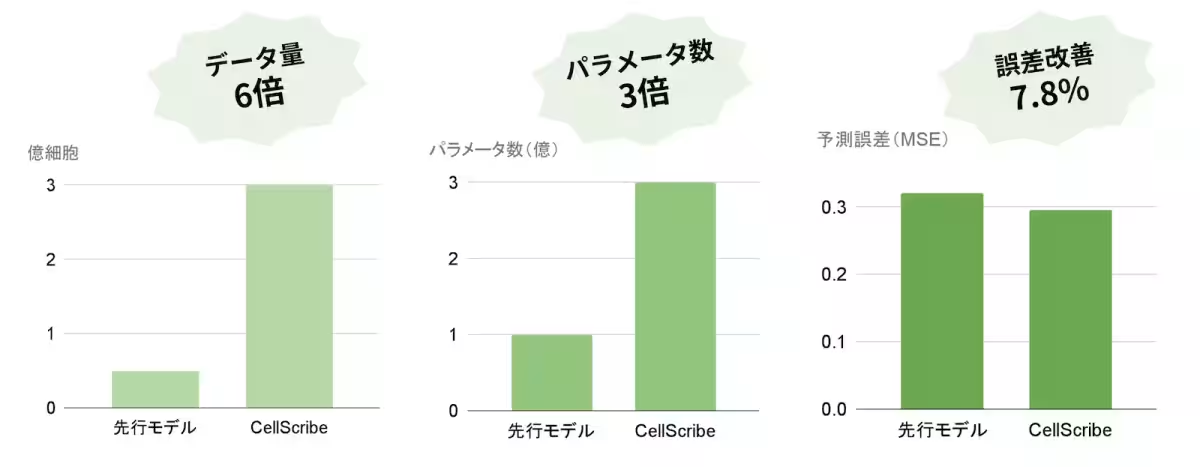
そこでヒューマノーム研究所が開発した「CellScribe」は、このニーズに応えるものとして生まれました。CellScribeは、約9億細胞のデータを分析し、3億パラメータを基にした基盤モデルを形成。その結果、既存モデルに比べて予測誤差を7.8%削減し、非常に高い精度を achieve しました。
CellScribeの仕組み
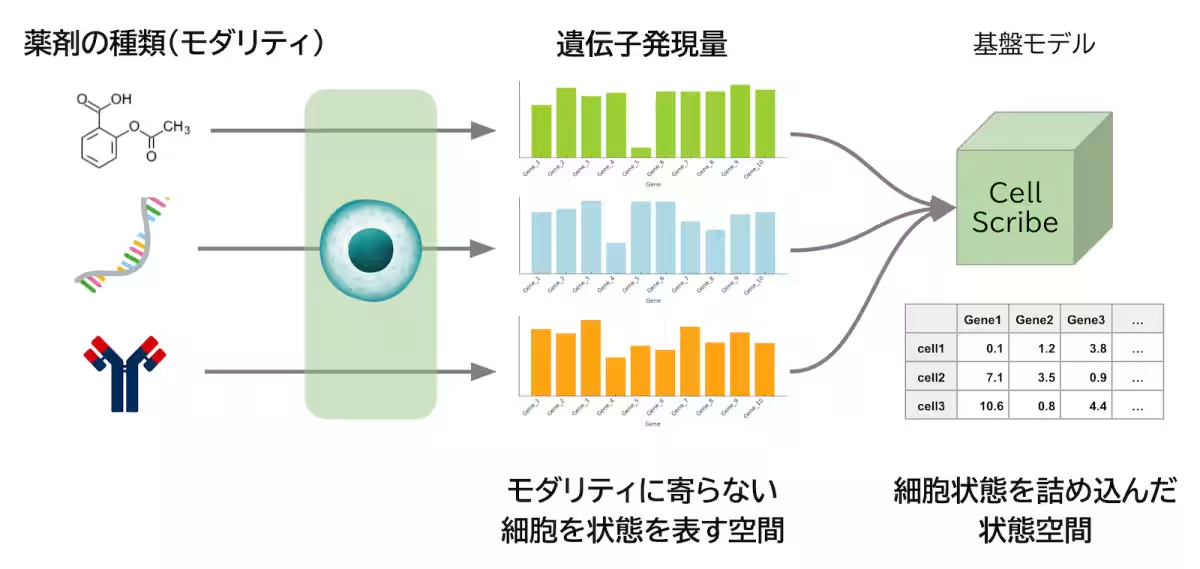
CellScribeは、遺伝子発現データを基に、細胞間の関係性を視覚的に捉える「細胞の地図」を生成します。この地図を通じて、得られたデータの特徴や傾向を把握することができ、さらに有望な創薬ターゲットや未知のルートの発見も期待できます。この技術は、創薬にかかる時間を大幅に短縮すると同時に、精度の高い予測を可能にします。
データ準備と性能向上
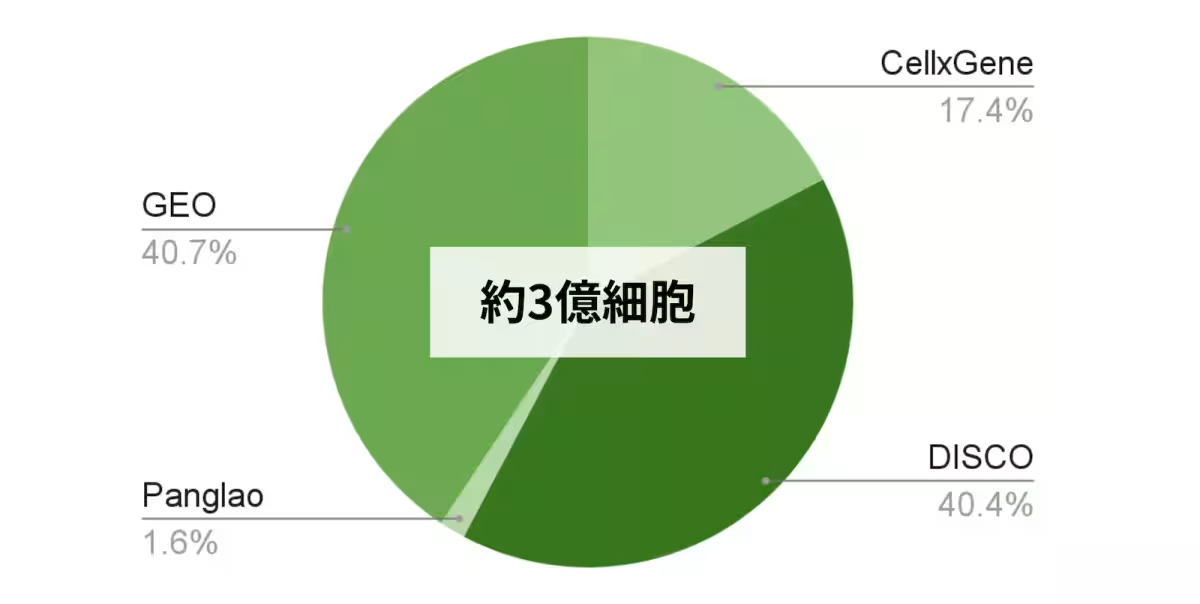
CellScribeの開発にあたり、公開データベース「CellxGene」などから9億細胞分の遺伝子発現データを収集しました。これに加えて、実験データのメタデータや高品質データの選別を行うことで、約3億細胞の高品質データセットを構築しました。これにより、未知のデータに対する高い汎化性能が得られています。
今後の展望
ヒューマノーム研究所は、今後もCellScribeの性能を向上させるために、シングルセル以外の実験データも取り入れた学習データの充実とモデルの改良を進めていく計画です。また、製薬企業やアカデミア、バイオ系スタートアップとの連携を強化し、実際の創薬研究や疾患メカニズムの解明に向けた具体的な応用事例の創出を目指します。
結論
CellScribeの開発は、新たな創薬研究の可能性を切り拓くものです。AI技術のさらなる進化によって、医療の未来がどのように変わるか、今から楽しみです。創薬コストの削減や新薬の開発効率化が期待され、生命科学分野でのAI活用がますます進むことでしょう。
会社情報
- 会社名
- 株式会社ヒューマノーム研究所
- 住所
- 東京都中央区築地2-4-10 SAテンハウス2階
- 電話番号
トピックス(科学)






【記事の利用について】
タイトルと記事文章は、記事のあるページにリンクを張っていただければ、無料で利用できます。
※画像は、利用できませんのでご注意ください。
【リンクついて】
リンクフリーです。