
新しいラテックス粒子の合成が検査キットの精度向上に貢献
近年、COVID-19やインフルエンザなど、さまざまなウイルス感染症への対応が求められています。その一環として、迅速かつ効率的に病原体を特定できる体外診断用医薬品(IVD)の開発が進んでいます。特に、ラテックス粒子を使用した免疫比濁法は、検体中の特定のタンパク質の量を測定するために広く利用されています。
この度、千葉大学大学院の研究チームが、タンパク質の非特異吸着を抑制する新しい高分子ラテックス粒子の合成手法を確立しました。研究によると、これらのラテックス粒子の表面に高密度で配置されたグラフト鎖が、意図しないタンパク質の付着をほぼ完全に防ぐことが可能であるとのことです。
感染症の診断および治療において、ウイルスや細菌を特定することが極めて重要です。特に、急性期や回復期の患者に対し、迅速に的確な治療法を決定するためには、助手的な診断手段が必要不可欠です。IVDは、身体への負担が少ない上に、簡便性、迅速性、定量評価が優れています。特にラテックス粒子を活用した免疫比濁法は、様々な疾患の診断において非常に有用です。
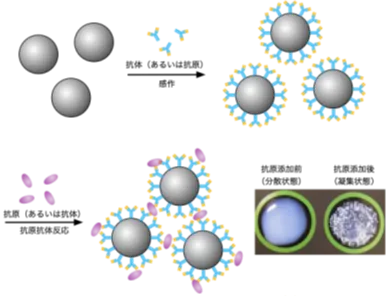
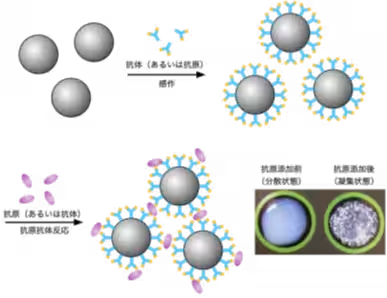
免疫比濁法は、ラテックス粒子が表面に固定化した抗体と、血清中に含まれる抗原との反応を利用して、濁り度を測定することで特定のタンパク質を定量的に評価します。しかし、ラテックス粒子の疎水性構造により、目的外のタンパク質が付着するファウリング現象が問題となっていました。これにより、誤った検査結果が生じる可能性があるため、ファウリング対策は重要な課題となっていました。
研究チームは、原子移動ラジカル重合(ATRP)という手法を用いることで、親水性の高分子鎖をラテックス粒子表面に導入し、非特異吸着を抑制する方法を模索していました。ただし、さらなる精度向上には、タンパク質が吸着しにくい構造の設計が求められていました。
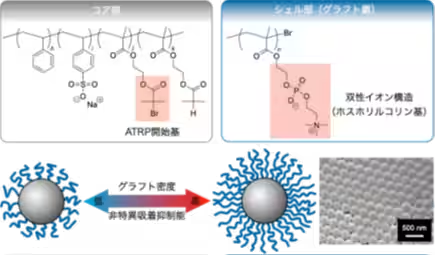
今回の研究では、直径約200nmの高分子ラテックス粒子を合成する際に、表面に特別な重合開始基を持たせることで、コア粒子の表面濃度を精密に制御する技術を確立しました。このラテックス粒子は、ポリスチレンを基材とし、双性イオン構造を有するモノマーを導入することによって、グラフト密度が高い特性を得ることができました。
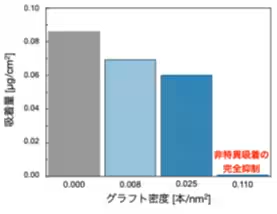
実験結果によれば、従来の粒子に比べて、グラフト密度が高密度に配置されたラテックス粒子では、特定のタンパク質であるウシ血清アルブミン(BSA)の非特異吸着が著しく低下しました。このことは、今後のIVD技術の向上に大きく寄与するものと考えられます。
新開発のコア-シェル型ラテックス粒子を用いることで、より精密な診断技術が実現し、個別化医療の展開が期待されます。免疫比濁法は、迅速、高感度、高特異性という特性を持つため、今後さまざまな分野での応用が見込まれます。この結果、我々の日常生活における医療の質を向上させ、感染症の早期発見や治療に大きく貢献することが期待されています。
今後もこの新技術を活用することで、診断精度を飛躍的に向上させることが可能になるでしょう。具体的には、特定の疾患に特化したターゲット分子を利用したIVDの開発が進むことで、医療従事者や患者にとっての診断の信頼性がさらに高まることが期待されています。
この度、千葉大学大学院の研究チームが、タンパク質の非特異吸着を抑制する新しい高分子ラテックス粒子の合成手法を確立しました。研究によると、これらのラテックス粒子の表面に高密度で配置されたグラフト鎖が、意図しないタンパク質の付着をほぼ完全に防ぐことが可能であるとのことです。
研究の背景
感染症の診断および治療において、ウイルスや細菌を特定することが極めて重要です。特に、急性期や回復期の患者に対し、迅速に的確な治療法を決定するためには、助手的な診断手段が必要不可欠です。IVDは、身体への負担が少ない上に、簡便性、迅速性、定量評価が優れています。特にラテックス粒子を活用した免疫比濁法は、様々な疾患の診断において非常に有用です。
免疫比濁法は、ラテックス粒子が表面に固定化した抗体と、血清中に含まれる抗原との反応を利用して、濁り度を測定することで特定のタンパク質を定量的に評価します。しかし、ラテックス粒子の疎水性構造により、目的外のタンパク質が付着するファウリング現象が問題となっていました。これにより、誤った検査結果が生じる可能性があるため、ファウリング対策は重要な課題となっていました。
研究チームは、原子移動ラジカル重合(ATRP)という手法を用いることで、親水性の高分子鎖をラテックス粒子表面に導入し、非特異吸着を抑制する方法を模索していました。ただし、さらなる精度向上には、タンパク質が吸着しにくい構造の設計が求められていました。
新技術の成果
今回の研究では、直径約200nmの高分子ラテックス粒子を合成する際に、表面に特別な重合開始基を持たせることで、コア粒子の表面濃度を精密に制御する技術を確立しました。このラテックス粒子は、ポリスチレンを基材とし、双性イオン構造を有するモノマーを導入することによって、グラフト密度が高い特性を得ることができました。
実験結果によれば、従来の粒子に比べて、グラフト密度が高密度に配置されたラテックス粒子では、特定のタンパク質であるウシ血清アルブミン(BSA)の非特異吸着が著しく低下しました。このことは、今後のIVD技術の向上に大きく寄与するものと考えられます。
今後の展望
新開発のコア-シェル型ラテックス粒子を用いることで、より精密な診断技術が実現し、個別化医療の展開が期待されます。免疫比濁法は、迅速、高感度、高特異性という特性を持つため、今後さまざまな分野での応用が見込まれます。この結果、我々の日常生活における医療の質を向上させ、感染症の早期発見や治療に大きく貢献することが期待されています。
今後もこの新技術を活用することで、診断精度を飛躍的に向上させることが可能になるでしょう。具体的には、特定の疾患に特化したターゲット分子を利用したIVDの開発が進むことで、医療従事者や患者にとっての診断の信頼性がさらに高まることが期待されています。



会社情報
- 会社名
- 国立大学法人千葉大学
- 住所
- 千葉県千葉市稲毛区弥生町1-33
- 電話番号
- 043-251-1111
トピックス(科学)







【記事の利用について】
タイトルと記事文章は、記事のあるページにリンクを張っていただければ、無料で利用できます。
※画像は、利用できませんのでご注意ください。
【リンクついて】
リンクフリーです。