
AI時代を見据えた医療機器ソフトウェア規制の全貌解説
AI時代の医療機器ソフトウェア規制に迫る
医療業界において、AI技術の進化はもはや避けられない現実となっています。それに伴い、医療機器ソフトウェア規制も新たな局面を迎えています。ここでは、最近公開された医療機器ソフトウェア規制に関する解説動画を基に、その概要や重要ポイントを詳しく掘り下げていきます。
1. 医療機器ソフトウェア規制の重要性
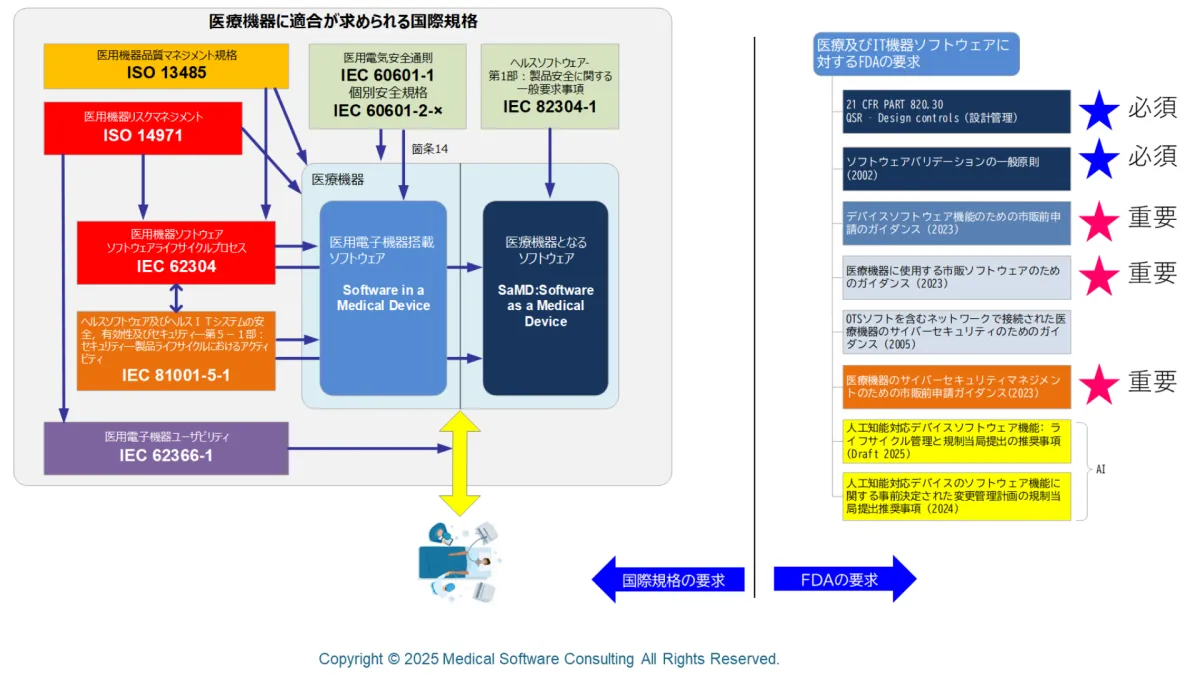
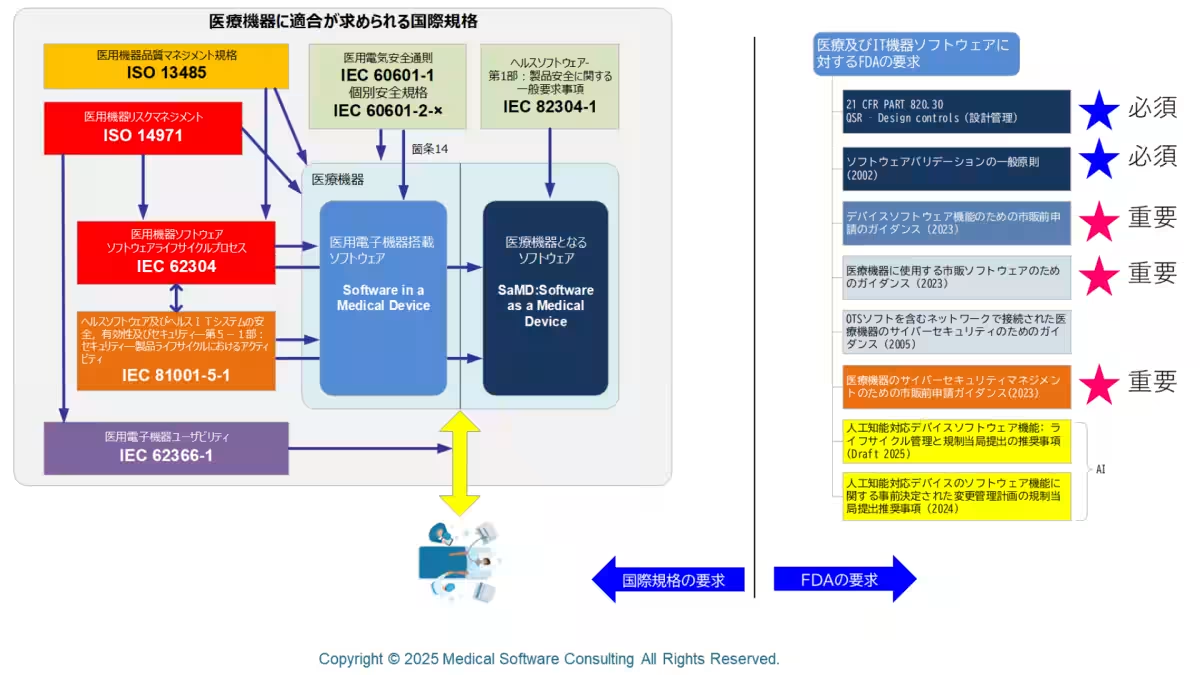
医療機器ソフトウェアは、デバイス全体の機能を支える核心的な要素です。これは、診断や治療における精度や安全性を確保するために欠かせないものとなっています。そのため、規制は非常に重要で、国際規格やFDAガイダンスに従った開発が求められています。
2. 最新の米国FDAガイダンス
Medical Software Consulting(MSC)が公開した動画では、米国FDAが発行するいくつかの医療機器ソフトウェア関連ガイダンスに触れています。特に、2023年版の市販前申請ガイダンスでは、スマートフォンやクラウドサービスと連携することで、AIを用いた医療機器の機能が複雑化している現状を反映し、規制対象が「ソフトウェア機能」へと移行しました。この変更は、よりリスクを適切に評価し管理するための重要なステップとされています。
3. AI医療機器の進化
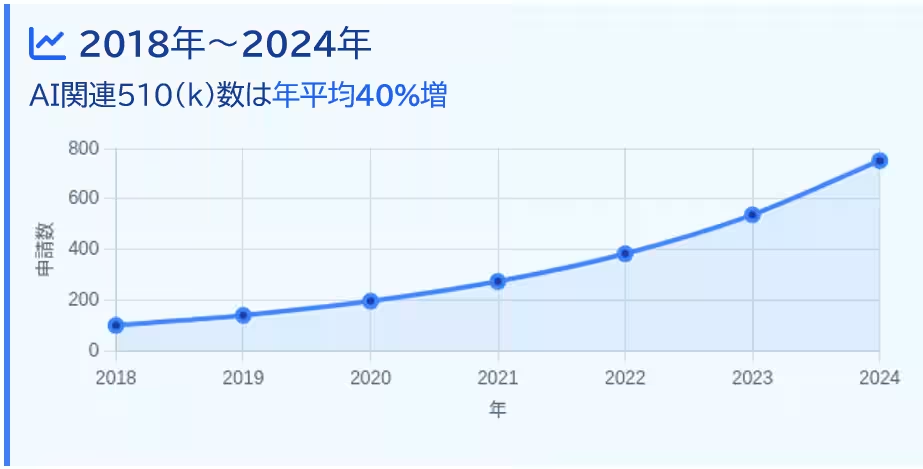
この状況下で、特に注目されるのはAI医療機器の市場とその規制です。2018年以降、AI関連の医療機器申請数は毎年約40%増加しています。中でも、放射線画像診断やECG解析などの分野において急速な進展が見られます。これにより、AIに特有のリスクやデータドリフトが顕在化し、適切な規制やガイダンスの必要性が高まっています。
4. 医療機器ソフトウェアの継続的な開発
FDAは、AI医療機器の将来のアップデート計画を事前に承認し、改善サイクルをスムーズに進めるためのPDCC(Predetermined Change Control Plan)を導入しています。この制度により、医療機器開発者は柔軟に仕様変更を行うことができ、より良いサービスを迅速に提供可能です。日本国内ではまだ整備が進んでいない部分もありますが、早急に学習を進めることが不可欠です。
5. MSCの取り組み
MSCは、AI医療機器ソフトウェアに対するガイダンスを視覚的に理解しやすくする解説動画を公開しており、企業の規制遵守をサポートしています。エンジニアや開発担当者は、短期間で最新規制をマスターすることができるため、積極的な利用が進められています。また、教育コンテンツの提供だけでなく、コンサルティングサービスも行い、すべてのニーズに応える体制を整えています。
6. 未来への展望
今後、医療機器ソフトウェアに関するさらなる動画も公開予定です。特に、規制の変遷や新たな技術への適応など、学びを深めるための情報を届けるために、継続的な取り組みが行われるでしょう。
医療機器の開発に携わる全ての方にとって、これらのガイダンスや情報は必須の教材となります。今後もMSCからの最新情報に注目していきましょう。


会社情報
- 会社名
- Medical Software Consulting
- 住所
- 電話番号
トピックス(IT)










【記事の利用について】
タイトルと記事文章は、記事のあるページにリンクを張っていただければ、無料で利用できます。
※画像は、利用できませんのでご注意ください。
【リンクついて】
リンクフリーです。