
AIを活用したタンパク質構造解析手法『DeepAFM』の新展開
新たな画像解析手法『DeepAFM』の開発
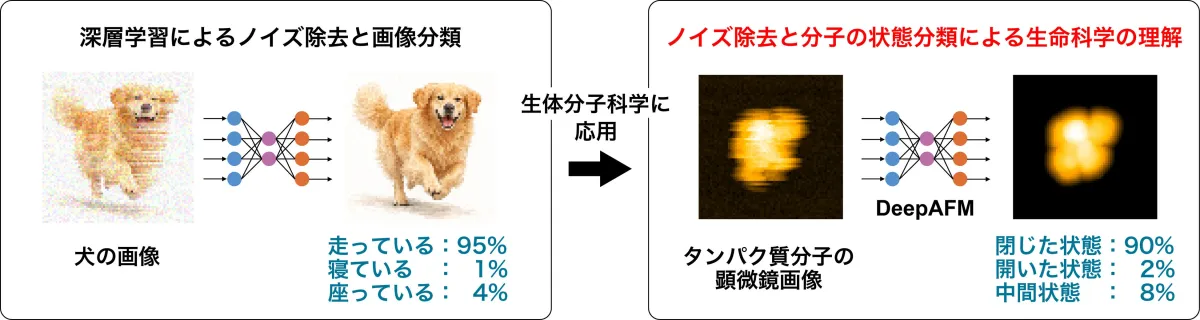
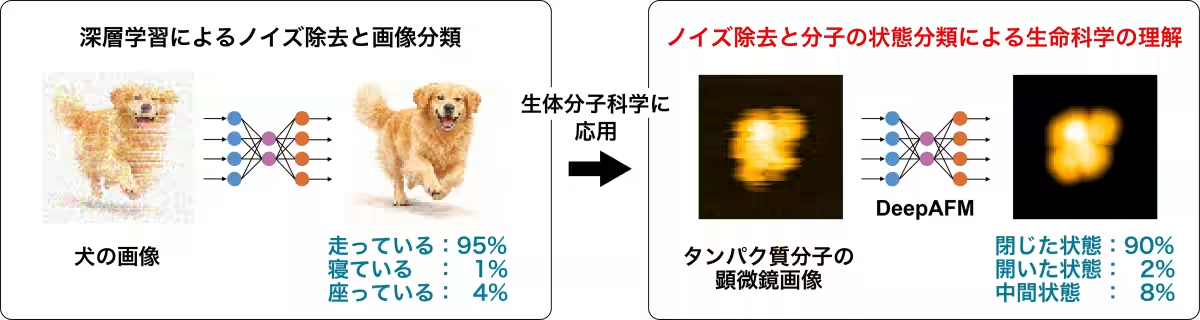
東京理科大学の森貴治准教授と佐藤克樹氏(2025年度修士課程修了)の研究グループが開発した新しい画像解析手法『DeepAFM』は、高速原子間力顕微鏡(HS-AFM)画像からタンパク質の構造状態を高精度に推定することを可能にします。
深層学習と分子シミュレーションの融合
『DeepAFM』は、分子シミュレーションによって生成された大量のデータと深層学習を駆使して、画像中のノイズを除去しながらタンパク質構造を正確に推定します。これは、通常のHS-AFM画像では解像度が低く、ノイズや歪みが伴うため、困難とされていたタンパク質の詳細な解析を実現します。
研究の背景とHS-AFMの特性
HS-AFMは、ナノメートルスケールの探針を振動させ、試料表面を高速に走査することによって、時間分解能の高い観察を実現しています。通常、タンパク質の構造は柔軟であり、多様性がありますが、従来の解析手法ではノイズの影響を受けやすく、信頼性が問われていました。そのため、深層学習を用いた新たなアプローチが求められていました。
『DeepAFM』の具体的な手法
本研究では、対象のタンパク質に分子動力学シミュレーションを行って多様な立体構造を生成し、人工的なAFM画像を作成します。これに状態ラベルを付与し、教師あり深層学習モデルを構築。実験画像にこのモデルを適用することで、ノイズ除去と状態分類の両方を同時に実現します。
実験結果とその重要性
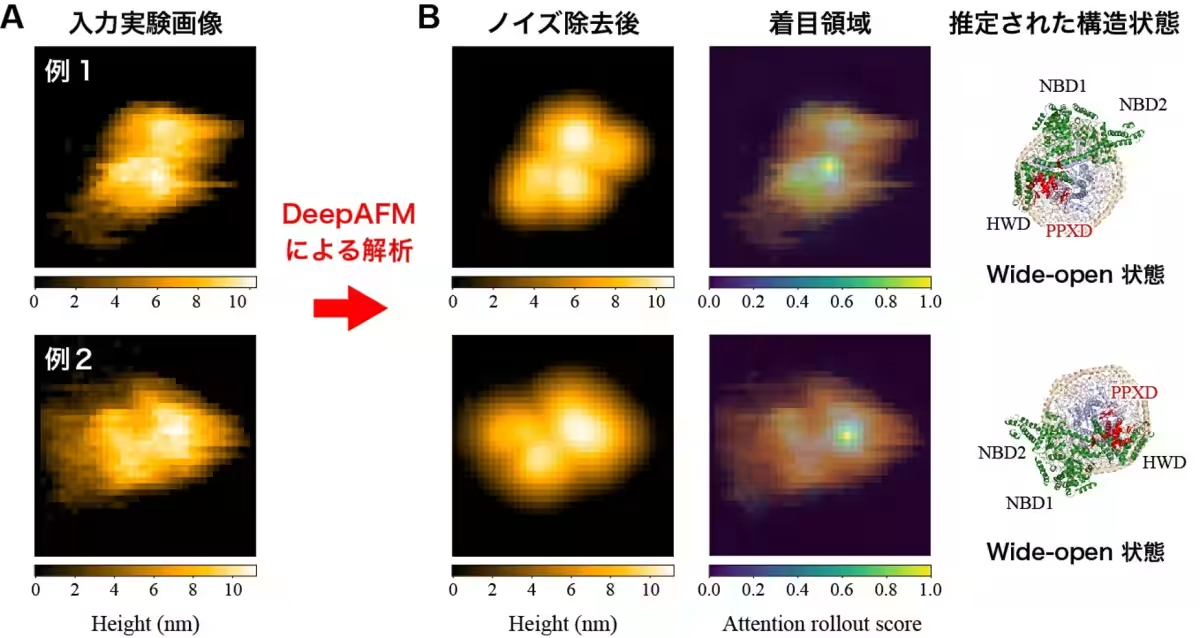
研究グループは、膜タンパク質のHS-AFM画像に対して『DeepAFM』を適用し、ノイズを効果的に排除した結果、タンパク質が持つ開閉動作に関連する構造状態を正確に推定しました。この結果は、他の実験結果でも異なりがなく、DeepAFMの有効性が確認されました。
今後の展望
本手法は、今後さまざまな生体分子系に応用されることで、生命科学のさらなる理解を進めることが期待されます。森准教授は、「本研究を通じて、シミュレーションとAIが人間の解析を効果的に支援する助けとなるでしょう」とコメントしています。また、この成果は国際学術誌に掲載される予定であり、今後の研究への影響が注目されています。
研究資金と支援
本研究は、日本学術振興会や革新的ハイパフォーマンス・コンピューティング・インフラなどの資金支援を受けて実施されました。特にスパコン『富岳』の活用が成果を大きく助けています。
結論
タンパク質構造を高精度に解析するための『DeepAFM』の開発は、生命科学の研究において画期的な進展を示すものであり、今後の応用が広がることで、より深い理解が期待されます。
会社情報
- 会社名
- 学校法人東京理科大学
- 住所
- 東京都新宿区神楽坂1-3
- 電話番号
- 03-3260-4271
トピックス(科学)





【記事の利用について】
タイトルと記事文章は、記事のあるページにリンクを張っていただければ、無料で利用できます。
※画像は、利用できませんのでご注意ください。
【リンクついて】
リンクフリーです。